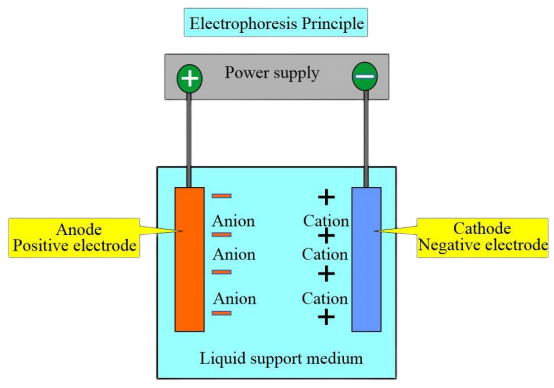
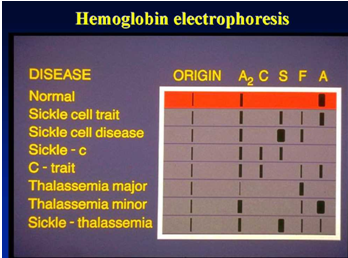
Principio do experimento
A electroforese da hemoglobina ten como obxectivo detectar e confirmar varias hemoglobinas normais e anormais.
Debido ás diferentes cargas e puntos isoeléctricos dos diferentes tipos de hemoglobina, nunha determinada solución tampón de pH, cando o punto isoeléctrico da hemoglobina é inferior ao pH da solución tampón, a hemoglobina leva unha carga negativa e migra cara ao ánodo durante a electroforese. Pola contra, a hemoglobina cunha carga positiva móvese cara ao cátodo.
Baixo unha determinada tensión e despois dun tempo de electroforese específico, as hemoglobinas con diferentes cargas e pesos moleculares presentan diferentes direccións e velocidades de migración. Isto permite a separación de zonas distintas e a posterior análise colorimétrica ou electroforética pódese realizar nestas zonas para cuantificar varias hemoglobinas. O método máis utilizado é a electroforese de membrana de acetato de celulosa de pH 8,6.
Dentro do citoplasma, os grupos etilenglicol (CHOH-CHOH) presentes en substancias glicóxenas ou polisacáridas (como mucopolisacáridos, mucoproteínas, glicoproteínas, glicolípidos, etc.) son oxidados polo ácido periódico e convértense en grupos aldehídos (CHO-CHO). Estes grupos aldehídos combínanse co reactivo incoloro de Schiff vermello violáceo, formando un colorante vermello púrpura que se deposita onde os polisacáridos están presentes na célula. Esta reacción coñécese como tinción periódica de ácido-Schiff (PAS), antes coñecida como tinción de glicóxeno.
Método de experimentación
Materiais:Acetato de celulosamembrana, aparello de electroforese(DYCP-38C e fonte de alimentación DYY-6C), Ferramenta de carga de mostras superior (pipeta), espectrofotómetro, cubetas colorimétricas, buffers.
Buffer:
(1) Tampón de pH 8,6 TEB: Pese 10,29 g de Tris, 0,6 g de EDTA, 3,2 g de ácido bórico e engade auga destilada a 1000 ml.
(2) Tampón borato: pesa 6,87 g de bórax e 5,56 g de ácido bórico e engade auga destilada a 1000 ml.
Procedemento:
Preparación de solución de hemoglobina
Tome 3 ml de sangue que conteña heparina ou citrato de sodio como anticoagulante. Centrifugar a 2000 rpm durante 10 minutos e descartar o plasma. Lavar os glóbulos vermellos tres veces con solución salina fisiolóxica (750 rpm, 5 minutos de centrifugación cada vez). Centrifugar a 2200 rpm durante 10 minutos e descartar o sobrenadante. Engade unha cantidade igual de auga destilada, despois engade 0,5 veces o volume de tetracloruro de carbono. Agite vigorosamente durante 5 minutos e, a continuación, centrifugue a 2200 rpm durante 10 minutos para recoller a solución de Hb superior para o seu uso posterior.
Remolando a Membrana
Cortar a membrana de acetato de celulosa en tiras de 3 cm × 8 cm. Molla-los en tampón de pH 8,6 TEB ata que estean completamente saturados, despois retiralos e sécalos con papel de filtro.
Detección
Use unha pipeta para localizar 10 μl da solución de hemoglobina verticalmente sobre a membrana de acetato de celulosa (o lado áspero), a uns 1,5 cm do bordo.
Electroforese
Verter a solución tampón de borato na cámara de electroforese. Coloque a membrana de acetato de celulosa co lado manchado no extremo do cátodo da cámara. Executar a 200 V durante 30 minutos.
Elución
Cortar as zonas HbA e HbA2, colocalas en tubos de ensaio separados e engadir 15 ml e 3 ml de auga destilada, respectivamente. Agite suavemente para eluír a hemoglobina completamente e despois mestura.
Colorimetría
Pon a cero a absorbancia usando auga destilada para a solución de elución e mide a absorbancia a 415 nm.
Cálculo
HbA2(%) = Absorbancia do tubo de HbA2 / (Absorbancia do tubo de HbA × 5 + Absorbancia do tubo de HbA2) × 100%
Cálculo de resultados experimentais
Intervalo de referencia para pH 8,6 TEB Tampón acetato de celulosa Electroforese: HbA > 95%, HbA2 1%-3,1%
Notas
O tempo de electroforese non debe ser demasiado longo. A membrana de acetato de celulosa non debe secarse durante a electroforese. Deter a electroforese cando a HbA e a HbA2 estean claramente separadas. A electroforese prolongada pode causar difusión de bandas e borrosidade.
Evite usar demasiada mostra. O exceso de líquido de hemoglobina pode provocar un desprendimento da banda ou unha mancha insuficiente, o que provoca niveis de HbA falsamente elevados.
Evitar a contaminación da membrana de acetato de celulosa con proteínas.
A corrente non debe ser demasiado alta; se non, as bandas de hemoglobina poden non separarse.
Inclúa sempre mostras de individuos normais e hemoglobinas anormais coñecidas necesarias como controis.
Beijing Liuyi Biotechnology fabrica o tanque de electroforese profesional para electroforese de hemoglobina que é o modeloDYCP-38CTanque de electroforese de membrana de acetato de celulosa e hai dous modelos de fonte de alimentación de electroforese dispoñibles para o tanque de electroforese de membrana de acetato de celulosaDYY-2CeDYY-6Cfonte de alimentación.
Mentres tanto, Beijing Liuyi Biotechnology ofrece membrana de acetato de celulosa para os clientes, e o tamaño da membrana de acetato de celulosa pódese personalizar. Benvido a pedirnos mostras e máis información.
A marca Beijing Liuyi ten máis de 50 anos de historia en China e a empresa pode ofrecer produtos estables e de alta calidade en todo o mundo. A través de anos de desenvolvemento, é digno da súa elección!
Agora estamos á procura de socios, tanto o tanque de electroforese OEM como os distribuidores son benvidos.
Se tes algún plan de compra dos nosos produtos, non dubides en contactar connosco. Podes enviarnos unha mensaxe ao correo electrónico[correo electrónico protexido]ou[correo electrónico protexido], ou chámanos ao +86 15810650221 ou engade Whatsapp +86 15810650221 ou Wechat: 15810650221
Hora de publicación: 20-09-2023